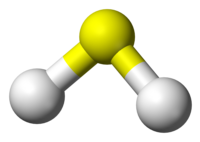
Hydrogensulfid
| Hydrogensulfid | |||||
|---|---|---|---|---|---|
| |||||
| Identifikatorer | |||||
| CAS-nummer | |||||
| SMILES | [H]S[H] | ||||
| Kjemiske egenskaper | |||||
| Formel | H2S | ||||
| Molar masse | 34,08 g/mol | ||||
| Utseende | Fargeløs gass, lukter råtne egg | ||||
| Tetthet | 1363 kg/m3 | ||||
| Smeltepunkt | −82,9 °C | ||||
| Kokepunkt | −61,8 °C | ||||
| Damptrykk | 1740 kPa (ved 21 °C) | ||||
| Løselighet | 4 g/dm (ved 20 °C) | ||||
| Mag. sus. | −25,5·10−6 cm3/mol | ||||
| nD | 1,000644 | ||||
| Dipolmoment | 0,97 D | ||||
| Termokjemiske egenskaper | |||||
| Dannelsesentalpi ΔfH | −21 kJ/mol | ||||
| Molar entropi S | 206 J mol−1 K−1 | ||||
| Varmekapasitet, C | 1.003 J K−1 g−1 | ||||
| Farer | |||||
| Hovedfarer | |||||
| Flammepunkt | −82,4 °C | ||||
| Tenntemperatur | 232 °C | ||||
| Eksplosjonsgrense | 4,3–46% | ||||
| LD50 | 713 ppm (rotte 1 time) | ||||
| Relatert | |||||
| Andre lignende forbindelser | Vann, Hydrogenselenid, Hydrogentellurid, Hydrogenpolonid, Hydrogendisulfid, Sulfanyl, Fosfin | ||||
Hydrogensulfid (H2S) er en fargeløs, giftig, brannfarlig gass ved romtemperatur med en karakteristisk, stikkende lukt av råtne egg. Gassen er noe tyngre enn luft.
Forekomst[rediger | rediger kilde]
Gassen dannes ved anaerob bakteriell nedbrytning av svovelholdige organiske forbindelser, eller ved reduksjon med sulfat. Eksempler der gassen dannes er i tankanlegg som septiktanker, og i slamansamlinger. Dette problemet oppstår også ofte i fiskebåter ved utilstrekkelig nedkjøling av industrifisk. Gassen dannes i stillestående vann, som ved myr- og sump-områder og kalles derfor ofte sumpgass. Gassen forekommer naturlig i råolje og naturgass, og ved oljeboring er dette et stort problem. Det dannes imidlertid raskt andre forbindelser da H2S er reaktivt og løselig i vann (H2O). Reaksjonen med vann er:
H2S + 4 H2O ⇒ H2SO4 + 4 H2(g)
der
- H2SO4 er svovelsyre, som er en sterk syre. I konsentrert væskefase er den tyktflytende og oljeaktig. I gassfase er den luktfri og uten farge.
- H2(g) er hydrogen i gassfase.
Syrer og salter[rediger | rediger kilde]
Svovelsyre (H2SO4 ) fortynnet med vann (H2O) er en svak toprotisk syre. Utviklingen er:[1]
H2SO4 + H2O ⇆ HSO4 + H3O+
HSO4 + H2O ⇆ SO42− + H3O+
der:
- HSO4 er hydrogensulfat.
- H3O+ er et hydronium-ion.
Den første likevekten er forskjøvet helt til høyre, men ikke den andre.
Saltene kalles sulfider. Disse er ofte tungt løselige. Hydrogensulfid danner to rekker salter, normale sulfider og hydrogensulfider. Eksempler er natriumsulfid Na2S, og natriumhydrogensulfid NaHS.
Industriell bruk[rediger | rediger kilde]
H2S benyttes i produksjon av svovel og svovelsyre, ved fremstilling av tungtvann og innen analytisk kjemi. Stoffet inngår også i produksjon av rayon, cellofan, papirmasse, plast, stål, gummi og ved garving av lær.
Helseeffekter ved eksponering[rediger | rediger kilde]
Ved høyt innhold av H2S i luften, er gassen dødelig.[trenger referanse]
Ved konsentrasjoner over 100 ppm lammes luktesansen slik at lukt og irritasjon ikke er pålitelige vern mot et helseskadelig nivå.
H2S opptas vesentlig ved innånding og gassen er giftig da den forhindrer kroppens utnyttelse av oksygen. H2S er en rasktvirkende gift og oppleves som irriterende selv i lave konsentrasjoner. H2S utskilles raskt fra organismen og akkumulerer ikke i kroppen.[trenger referanse]
Irritasjon og betennelsesreaksjoner kan oppstå ved lave konsentrasjoner (under 10 ppm). Vedvarende eksponering kan gi såkalte "gassøyne" med kløe, irritasjon og tåreflod. Det kan oppstå permanente skader, men symptomene forsvinner gjerne når eksponeringen opphører. Luktubehag oppstår ved en konsentrasjon på 0,13-30 ppm. Ved 50 ppm H2S kan det inntre markert tørrhet og irritasjon av nese og hals. Vedvarende eksponering kan forårsake rennende nese, hoste, heshet, pustebesvær og kjemisk lungebetennelse. En konsentrasjon på 200-250 ppm kan gi alvorlig irritasjon og etter hvert inntrer systematiske symptomer som nevnt over. Vedvarende eksponering kan medføre lungeødem og eventuelt død etter 4-8 timers eksponering. Ved 300-500 ppm opptrer de samme symptomene som nevnt over, men raskere og mer alvorlig. Død inntrer etter 1-4 timer ved 300 ppm og etter ½-1 time ved 500 ppm. Høye konsentrasjoner av H2S damp kan virke irriterende på hud.[trenger referanse]
Muligvis kan langvarig eksponering for H2S gi varig skade i nervesystemet.[trenger referanse] Virkningen av H2S på de ulike konsentrasjonsnivåer er avhengig av eksponeringstiden og om det foreligger en enkeltstående kortvarig eksponering eller gjentatte kortvarige eksponeringer. Flere undersøkelser tyder på at gjentatte kortvarige høye eksponeringer er alvorligere enn kronisk lav eksponering. I avløpsvirksomheten har undersøkelser vist at en har jevnt over lav eksponering for H2S (ofte < enn 1 ppm) samtidig som en har sporadisk høyere eksponeringer knyttet til spesielle arbeidsprosesser. Disse prosessavhengige toppeksponeringene vil derfor være av betydning.[trenger referanse]
Arbeidstilsynets normer for forurensning i arbeidsatmosfære er 10 ppm og 15 mg/m³ (takverdi).[2]
Du bør aldri bruke informasjon fra Internett, inkludert dette kapittelet i Wikipedia, som eneste kilde til avgjørelser eller tiltak i helsemessige spørsmål. Ved helsespørsmål spør relevant autorisert helsepersonell, og ved dyresykdom bør du rådspørre veterinær.
Nedbryting av konstruksjoner[rediger | rediger kilde]
Hydrogensulfid selv i små konsentrasjoner kan påvirke utmattingslevetiden på sveiser i stål. Flere testresultater tilsier at utmattingslevetiden kan bli redusert betydelig.[3] Fenomenet er nært beslektet med effekten av fri hydrogen. Sjøvann i tillegg til H2S vil redusere levetiden ytterligere.[4] En kortvarig påvirkning av H2S ser derimot ikke ut til å ha negative effekter.[5] Fritt hydrogen vil øke sprekkdannelsen for korrosjonsbeskyttede konstruksjoner. Spesielt for høyfast stål og høye belastninger vil sterk grad av katodisk vern kunne gi redusert levetid. Hydrogenatomene vil gjøre materialet mer sprøtt fordi atomene vil samle seg der spenningene er størst, og gjøre materialet lokalt sprøtt. Konstruksjoner som er utsatt for H2S har større tilgang på hydrogenatomer enn normalt.
Det er tatt opp mange eldre ankerkjettinger fra flytende produksjonsplattformer til havs (FPSOer). Mange av kjettingene har omfattende gropkorrosjon, som er forårsaket av bakterier som lever i havbunnen uten tilgang på oksygen, og som produserer syrer. De betegnes som sulfatreduserende bakterier (SRB) og prosessen som mikrobiologisk indusert korrosjon (MIC). Det er i flere tilfeller gjort omfattende testing, og de er sammenliknet med ny kjetting. Testingen viser at korrosjonen reduserer utmattingslevetiden betydelig.[6]
Det måles rutinemessig H2S i lagercellene på betongplattformer. Konsentrasjonen av H2S i lagercellene (opp til 4000 ppm) er målt til vesentlig større enn i brønnstrømmen (300-400 ppm). Gass lages av bakterier, og de produserer trolig gassen i lagercellene i overgangen mellom vann og olje. H2S-gass fra bakterier er også knyttet til produksjon av syrer.[7] Syrene kan angripe stålkonstruksjoner og -utstyr, og fra kloakkledninger vet en at slike syrer også ødelegger betong.[8]
Referanser[rediger | rediger kilde]
- ^ Pedersen, Bjørn. (2019, 21. april). svovelsyre. I Store norske leksikon.Hentet 30. januar 2020
- ^ Arbeidstilsynet: Administrative normer for forurensning i arbeidsatmosfære, 2003. Bestillingsnummer 361.
- ^ McMaster Fraser, Hugh Thompson, Michelle Zhang, David Walters and Jonathan Bowman: Sour service corrosion fatigue testing of flowline welds, OMAE 2007-29060, 2007.
- ^ Ebara Ryuichiro, Yoshikazu Yamada, Hiroshi Yajima, Akira Fushimi og Eiichi Watanabe: Corrosion fatigue strength of ship structural plates in sour crude oil, Mitsubishi heavy industries Technical review, volume 32, number 1, 1995.
- ^ Spoerker, H.F., Havlik, W., Jellison, M.J (2009 ): What really happens to high-strength drill pipe after exposure to sour gas environment?[død lenke], Drilling Contractor.
- ^ Se for eksempel Gabrielsen, Ø., Larsen, K., Dalane, O., Lie, H. B., & Reinholdtsen, S. A.: Mean Load Impact on Mooring Chain Fatigue Capacity: Lessons Learned From Full Scale Fatigue Testing of Used Chains. OMAE, Glasgow, juni 2019.
- ^ Arne Kvitrud, Terje L. Andersen og Marita Halsne: Rapport etter tilsynet med tilstanden på betongunderstellet på Gullfaks C, Petroleumstilsynet, 2020.
- ^ Se Ulla Kjær: Beton i aggressivt miljø, Beton-teknik nr. 2/03/1974, side 3ff, Lars Hjort: Betonrørs holdbarhed, Beton-teknik nr. 5/02/1982, side 2f og Reza Javaherdashti: A brief review of general patterns of MIC of carbon steel and biodegradation of concrete. IUFS Journal of Biology 68.2 (2009), side 65-73.
Eksterne lenker[rediger | rediger kilde]
- International Chemical Safety Card 0165
- Concise International Chemical Assessment Document 53
- National Pollutant Inventory – Hydrogensulfid faktaark
- NIOSH Lommeguide til kjemiske katastrofer
- MSDS sikkerhetsark
- Abstrakt om H2S i kroppen av P. Kamoun
- Computational Chemistry Wiki
- NACE Arkivert 19. juni 2010 hos Wayback Machine. (National Association of Corrosion Epal)