Infrarød spektroskopi
Infrarød spektroskopi er en analysemetode for å identifisere og kvantifisere materie(stoff) og forbindelser. Den utnytter det forhold at molekyler vibrerer ved at de kovalente bindingene strekkes og bøyes. De fleste molekyler har en eller flere vibrasjoner med frekvenser som ligger i den infrarøde delen av det elektromagnetiske spektrum. Ved å sende infrarød stråling gjennom en forbindelse vil de lysfrekvensene som er lik molekylvibrasjonsfrekvensene i forbindelsen absorberes eller hindres i å trenge gjennom prøven.
Intensiteten av disse lysfrekvensene avtar. Disse intensitetsendringene gir grunnlag for å finne forbindelsens infrarøde spektrum. En hver forbindelse har sitt unike infrarøde spektrum, som et fingeravtrykk. Infrarød spektroskopi foregår ved å sende mange infrarøde lysbølger samtidig mot prøven. Endringene i lysbølgene etter at disse har trengt gjennom eller blir reflektert fra prøven måles. Deretter foretas en omregning fra tidsområdet til frekvensområdet. Omregningen kalles Fouriertransformasjon, etter den franske matematikeren Jean Baptiste Joseph Fourier.
Teori[rediger | rediger kilde]
Molekyler absorberer infrarød stråling med en gitt frekvens dersom det eksisterer en energiovergang, ΔE, i molekylet slik at ΔE = hν = hc/λ.
E = strålingsenergi,
h = Plancks konstant,
ν = frekvens av stråling,
c = lys(stråle)hastighet og
λ = bølgelengde av stråling.
Overgangene som gir opphav til infrarød absorpsjon skyldes vibrasjoner i molekylet. Molekylvibrasjonene må medføre en netto endring av molekylets dipolmoment. Dipolmoment er ubalanse i elektrisk ladningsfordeling i molekylet.
I et vannmolekyl (H2O) vil det elektronegative oksygenatomet trekke til seg elektroner slik at det oppstår en negativ ladning der. Ved de to hydrogenatomene vil elektrontettheten være lav slik at atomkjerneladningen gjør dette til den positivt ladede delen av vannmolekylet. Vannmolekylet er en permanent, kraftig dipol.
Vibrasjoner som gir opphav til infrarød absorpsjon kan deles i to typer:
-
Strekkvibrasjon langs kovalent binding som ikke endrer bindingens vinkel
-
Deformeringsvibrasjon som medfører endring av bindingsvinklen
Det skal mer energi til for å strekke en binding enn å bøye den. Absorpsjonbånd som skyldes strekkvibrasjoner opptrer derfor ved høyere bølgetall enn absorpsjonbånd som skyldes deformasjon av den samme bindingen. Hookes lov sier at vibrasjonsfrekvensen for en binding øker når bindingsstyrken, k, øker og når den reduserte massen, m, av vibrasjonssystemet avtar:[1]. Den reduserte massen er gitt som [2] der m1 og m2 = massene til de to atomene som utgjør vibrasjonssystemet.
Elektromagnetisk stråling beskrives vekselvis som et bølgefenomen eller en fotonstrøm, ikke ulikt vann. Vann kan opptre som bølgene på havet og som regndråper (som partikler) fritt etter Stephen Hawking
-
Bølgefenomen, periodisk vekslende elektrisk/magnetisk felt
-
Fotonstrøm med energi E = hν.
En Natrium-metallplate trenger en strålingsenergi på minst 2 elektronvolt (eV) for at elektroner skal bli slått løs. Energien til de frigjorte elektronene følger frekvensen av bestrålingen. Energien til og farten på elektronet slått løs av fiolett lys er derfor høyest.
Karakteristiske parametere for elektromagnetisk stråling.[rediger | rediger kilde]
Energien i det elektromagnetiske spektrum er gitt ved sammenhengen mellom bølgelengde og frekvens; E = hν = hc/λ ; h er Plancks konstant 6,6256x10-34 Js
Fart av stråling = c, angis i meter per sekund m/s, c = λν
Bølgelengde = λ, angis i meter
Frekvens = ν, svingninger per sekund, angis i Hertz (Hz) eller 1/s
Bølgetall = 1/cm = 1/λ, cm−1 resiprok centimeter
Nærinfrarød/infrarød del av det elektromagnetiske spektrum er;
| Område | NIR | IR | |
|---|---|---|---|
| Bølgelengde | 780 nm | 2500 nm | 50000 nm |
| Bølgetall, cm−1 | 12800 | 4000 | 200 |
| Frekvens, Hz | 3,8*1014 | 1,2*1014 | 6*1012 |
| Mest benyttet | |||
| Bølgelengde | 1100 nm | 2500 nm | 15000 nm |
| Bølgetall, cm−1 | 10000 | 4000 | 670 |
Fouriertransformering[rediger | rediger kilde]
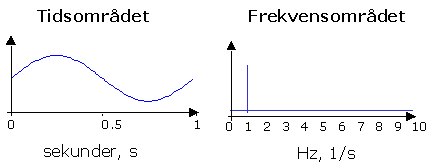
Lysstråling med kun en bølgelengde har bare en frekvens og ser ut som følger i henholdsvis tidsområdet og frekvensområdet.
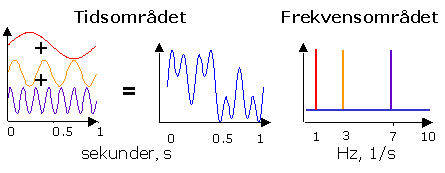
Lysstråling satt sammen av tre bølgelengder har kun tre frekvenser
I infrarøde måleinstrumenter er det tusenvis av bølgelengder som gir tusenvis av frekvenser
FTIR virker slik[rediger | rediger kilde]
Infrarøde frekvenser er om lag 1013 Hz. Digitalisering av så høye frekvenser er mer enn problematisk. For å klare dette gjøres en modulering eller flytting av frekvensene i det infrarøde lyset til et frekvensintervall som er håndterbart for digitalisering. Modulering av høyfrekvente signaler skjer også i vanlig FM radio, frekvensmodulering. For eksempel vil NRK P3 som sender en bærefrekvens på 99.0 megacycler/MHz bli modulert til omtrent 10.7 MHz. Moduleringen skjer i en såkalt blandekrets. Resten av de elektroniske komponentene i en radio bruker så det modulerte signalet som har om lag ti ganger lavere frekvens enn inngangssignalet på 99 MHz til å produsere lydsignaler.
De infrarøde frekvensene er så høye at man ikke klarer å modulere dem elektronisk. Moduleringen skjer derfor mekanisk ved å bruke et såkalt interferometer.
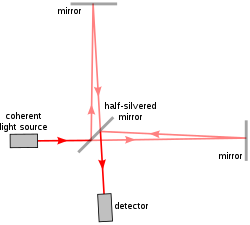
Et interferometer sørger for den infrarøde strålingen reflekteres tilbake på seg selv via to speil. Da oppstår enten utslokking eller forsterkning av lysbølgene (negativ eller positiv interferens).
Et av speilene står i ro, det andre beveger seg med kjent hastighet. Det medfører at intensiteten på signalene som treffer detektoren svinger mye seinere enn de originale IR signalene. Interferometeret minsker frekvensen med en faktor på om lag 1010, faktisk ned i lydområdet. Deretter skjer den kjente og kjære Fouriertransformeringen fra tidsområdet til frekvensområdet.
Helium-Neon lasere sender ut monokromatisk rødt lys og brukes som intern standard i FTIR instrumenter. Den ene frekvensen dette gir brukes for å sikre at hvert sveip med det bevegelige speilet starter til rett tid hver gang, slik at flere målesveip kan legges sammen før svært gode gjennomsnittsspektra beregnes.
FTIR brukes slik[rediger | rediger kilde]
I avsnittene over er det vist hvordan man produserer signalene i IR instrumenter. Disse signalene er ikke klare til bruk. FTIR instrumenter er såkalte enkeltstråleinstrumenter. Dvs. at et såkalt bakgrunnspekter og spekteret av prøven måles hver for seg.

Vanligvis måles det såkalte bakgrunnsspekteret først (blå). I dette spektrumet sees signaler fra vanndamp og karbondioksidgass og instrumentets optiske deler. Den krumme formen skyldes kaliumbromid som brukes i stråledeleren i interferometeret. H2O og CO2 skyldes at laboranter puster ut disse gassene, og at de finnes naturlig i atmosfæren.
Deretter puttes prøven som skal studeres på plass i målekammeret. Spekteret som nå kommer ut (lilla) etter Fouriertransformering inneholder signaler fra prøven i tillegg til bakgrunnen, som er den samme som før. Målingene av de to enkeltstrålespektrene er da avsluttet og det som gjentår er å fjerne bidraget av bakgrunnen i prøvespektrumet. Ved å dividere spekteret som inneholder signaler fra både prøve og bakgrunn med spekteret som kun inneholder bakgrunnssignaler får man et spektrum som kun inneholder signaler fra prøven (rød).
Kjært barn har mange navn og bakgrunnsspekteret kalles også instrumentprofilen eller referansespektrum. Prøvens infrarøde spektrum (rød) er nå klar til bruk i kvalitativ analyse, og etter en liten omregning er det klar til bruk i kvantitativ analyse. Kvalitativ analyse er å identifisere hvilken forbindelse/stoff/analytt man har med å gjøre. Kvantitativ analyse er å bestemme mengden man har av en eller flere forbindelse(r)/stoff/analytt(er).
Kvalitativ infrarød analyse[rediger | rediger kilde]
Når man har målt et IR-spekter, må man identifisere den kjemiske forbindelsen. Ulike deler av molekylet, såkalte funksjonelle grupper, gir opphav til vibrasjoner med ulike frekvenser. Ved å lese av antall signaler og deres posisjoner og høyder kan forbindelsen identifiseres.

I figuren er det vist hvilke molekylbiter, eller funksjonelle grupper, som er identifisert i spektrene av metanol og etanol. Settes puslespillene sammen får man molekylstrukturene som er vist på venstre side i figuren. Legg merke til at tilnærmet like molekyler gir tilnærmet like spektra. Det finnes mange korrelasjontabeller for funksjonelle grupper og absorpsjons-posisjonene deres. I tabellen er det vist noen av de mest karakterisktiske funksjonelle grupper med tilhørende frekvenser.
| Bølgetall, cm−1 | Vibrasjon | Forbindelse |
|---|---|---|
| 3500–3300 cm−1 | N–H strekk | aminer |
| 3500–3200 cm−1 | O–H strekk | alkoholer, en bred, stor topp |
| 3100–3000 cm−1 | C–H strekk | alkener |
| 3000–2850 cm−1 | C–H strekk | alkaner |
| 1760–1665 cm−1 | C=O strekk | ketoner, aldehyder, estere |
| 1680–1640 cm−1 | C=C strekk | alkener |
Kvantitativ infrarød analyse[rediger | rediger kilde]

Spørsmålet som besvares i kvantitativ analyse er; hvor mye av bestemte(e) forbindelse(r) finnes i prøven! I IR-spektroskopi følger, etter enkle omregninger, den målte signalstørrelsen mengden av favorittstoffet, og lengden på lysveien. Dobles mengden eller konsentrasjonen av favorittstoffet i prøven, dobles signalstørrelsen. Fordobles lysveien, fordobles signalstørrelsen! Fordobles både lysvei og konsentrasjon, blir signalstørrelsen firedoblet. Dette følger Beer-Lamberts lov.
Å bestemme mengde etanol løst i metanol er enkelt. I forrige avsnitt ble det vist at IR-spekteret til etanol inneholder en topp ved 880 cm-1 som ikke finnes i metanolspekteret. En slik topp kalles selektiv. At toppen er selektiv betyr at det er en, og bare en, forbindelse som er opphav til signalet ved en gitt bølgelengde.
Lages prøver med kjente blandingsforhold mellom etanol og metanol, kan en såkalt kalibreringskurve lages ved å tegne inn signalstørrelsen av den selektive toppen for etanol mot mengden etanol. Deretter tegnes inn, eller regnes ut, den beste beine linjen mellom disse punktene. Dette er kalibreringskurven.

Måles en prøve med ukjent blandingsforhold etanol/metanol finnes mengde etanol slik; Mål høyden på den selektive etanoltoppen, og merk denne av på den loddrette (y) aksen. Finn det tilhørende kryssningspunktet med kalibreringskurven. Trekk en loddrett strek ned til den vannrette (x) aksen. Les av volumprosent etanol i den ukjente prøven på den vannrette aksen. Det finnes mange tilfeller hvor dette ikke virker. Årsaken kan være at selektive topper ikke finnes. Forurensing av prøvene er en annen. Da finnes det et ukjent antall ukjente forbindelser med ukjente spektra i prøven. For å identifisere og kvantifisere alle forbindeler i slike prøver kan anvendelse av såkalt multikomponentanalyse være nyttig.

Måleteknikker i infrarød spektroskopi[rediger | rediger kilde]
Som nevnt over utføres to målinger for hvert infrarøde spekter av en prøve.

Transmittans[rediger | rediger kilde]
Transmittans er den eldste og mest kjente teknikken. Den krever enkle måleceller. Prøven må være gjennomsiktig for infrarød ståling, og blir plassert direkte i prøvekammeret på ett infrarødt spektrometer i en dertil egnet målecelle. Infrarød stråling blir sendt igjennom prøven og energien av den infrarøde strålingen som går gjennom prøven blir målt. Dermed er prøvens infrarøde spektrum funnet.
Definisjoner[rediger | rediger kilde]
Transmittans T = I / I0
er et mål på hvor mye av strålingen som slipper gjennom en prøve og finnes som forholdet mellom strålingsintensiteten, I, av lyset som treffer detektor etter å ha passert gjennom prøven og intensiten av strålingen, I0, som treffer detektoren uten å være hindret av prøven. (Prøvespektrum dividert på bakgrunnsspektrum) Signalstørrelsen er ikke direkte proporsjonal med konsentrasjonen c, av IR-absorberende molekyler i prøven.
- Absorbans A = - logT = log(1/T) = log(I0/I)
er den negative logaritmen av transmittansen. Det er et mål på hvor mye av strålingen som absorberes av IR-aborberende molekyler i prøven. Sammenhengen er slik at hvis en prøve absorberer 25 % av strålingen ved en gitt bølgelengde, er transmittansen ved denne bølgelengden 75%. Signalstørrelsen er direkte proporsjonal med konsentrasjonen c, av IR-aborberende molekyler i prøven.
- Beer-Lamberts lov A = ecl
er grunnlaget for kvantitative bestemmelser
- A = absorbans,
- e = molar absorbtivitet (1/(M cm))
- c = konsentrasjonen av IR-absorberende molekyler i prøven (M = mol/liter)
- l = veilengde ( cm) stråling i prøven
Prøvetyper[rediger | rediger kilde]
Infrarøde spektra av god kvalitet kan måles for en rekke typer prøver ved hjelp av transmisjon. Transmisjonsteknikken kan benyttes alene eller i kombinasjon med mikroskop og måleceller for væsker eller gasser for analysere blant annet væsker, gasser, organisk pulver i tablett- eller utrørt form, termoplastisk pulver, løslige polymerer og tynne polymerfilmer.

Diffus refleksjon[rediger | rediger kilde]
Når infrarød stråling blir fokusert på finmalte prøvepartikler vil den innsendte strålingen oppføre seg på flere måter. Den kan bli reflektert direkte fra partikkelens overflate uten å trenge inn i denne. Strålingen kan foreta mange påfølgende refleksjoner fra overflaten til mange partikler uten å trenge inn i disse. Diffus refleksjon oppstår når den innsendte strålingen trenger inn prøvepartiklene og siden blir spredd i prøven
En diffus refleksjonsmålecelle fokuserer innsendt infrarød stråling på en prøvekopp fylt med en blanding av prøvepartikler og et infrarødt gjennomsiktig materiale som til dømes kaliumbromid. Infrarød stråling blir reflektert, absorbert og spredd i prøven og den delen av strålingen som når overflaten av prøven blir via speil sendt til en detektor. Før prøvepartiklene måles er det vanlig å måle et bakgrunnsspektrum av kun det infrarøde gjennomsiktige materiale. Ved korrekt prøvepreparering kan kvantitative målinger foretas.
Definisjoner[rediger | rediger kilde]
Reflektans R = I/I0
er et mål på hvor mye av strålingen som reflekteres av en prøve. Det er forholdet mellom strålingsintensiteten, I, av lyset som treffer detektor etter refleksjon fra prøven og intensiten av strålingen, I0, som treffer detektoren uten å være hindret av prøven.
Log (1/R) = - logR = log(I0/I)
er et mål på hvor mye av strålingen som absorberes av IR-aborberende molekyler i prøven i et refleksjonsforsøk. Sammenhengen er slik at hvis en prøve absorberer 25 % av strålingen ved en gitt bølgelengde, er reflektansen ved denne bølgelengden 75%. Dette brukes i kvantitativ spektroskopi.
En annen mye brukt enhet er Kubelka-Munk enheten. Kubelka-Munk foretrekkes fordi det eliminerer bølgelengdeavhengige speilrefleksjonseffekter, som redusere analysenøyaktigheten.
KM = (1 - R)2/2R
For å kunne bruke denne må man fortynne prøven med til dømes KBr. Konsentrasjonen må være lav, i området 1 – 5% prøve til 99%- 95% fortynningsmateriale (eng: matrix) etter vekt. Alt pulver må være finmalt (anbefalt partikkelstorleik 2 – 5 mikrometer ). Pulverblandingen må være homogen og prøvetykkelsen minst 3 mm. Om det ikke er mulig å følge disse kriteriene brukes log (1/R).
Det er vanlig å benytte diffus refleksjon til analyse av både organiske og uorganiske prøver som kan finmales (< 10 mikro m) og blandes med en infrarød gjennomsiktig pulvermatrise som KBr.

Dempet totalrefleksjon[rediger | rediger kilde]
Dette er en refleksjonsteknikk. En infrarød lysstråle blir sendt gjennom et prisme som er gjennomsiktig for infrarød stråling. Krystallen må ha høyere brytningsindeks enn prøven det skal måles på. Den interne refleksjonen av den infrarøde strålingen i krystallen danner en kortlivet bølge som strekker seg ut fra krystallens overflate, og inn i en prøve som er i god kontakt med krystallen.
I områder av det infrarøde spekteret hvor prøven absorberer energi vil den flyktige bølgen bli dempet. Dermed oppstår endringer i den infrarøde strålingen som kommer ut i motsatt ende av krystallen. Endringene måles av en detektor og danner grunnlaget for å beregne prøvens infrarøde spektrum. Vanlige krystaller er germanium (Ge), zinkselenid (ZnSe) og diamant (C).
ATR er nyttig for prøver som absorberer mye eller er tjukke, for eksempel prøver som inneholder svart karbon og væsker som inneholder vann. Slike prøver gir ofte svært intense, og ubrukelige, topper når de måles ved hjelp av infrarød transmisjon. ATR teknikken kan benyttes på slike prøver fordi intensiteten i den kortlivete bølgen avtar raskt med avstanden fra krystallens overflate. Dette medfører at teknikken er lite følsom for ulike prøvetjukkelser. Andre typer fast materiale som er velegnet for å måle ved hjelp av ATR er homogene faste prøver, overflatelaget på flerlags prøver eller belegget på en fast prøve. En forutsetning for suksess er at prøven er flat nok eller så fleksibel at det er god kontakt mellom den og krystallen. I tillegg er ATR en enkel teknikk for væskeanalyse fordi målingen trenger kun en dråpe av væsken på krystallen. Bruk av diamantkrystall krever omtrent ingen prøvepreparering.
Historie[rediger | rediger kilde]
Prinsipper og metoder i utviklingen av spektroskopianalyse i det nær og midtre infrarøde området.
- År
- 1800 William Herschel påviste IR stråling med et forsøk du kan gjøre hjemme en solskinnsdag.
- 1880/82 Albert A. Michelson konstruerte det første interferometeret.
- 1882 Abney og Festing fotograferte spektra av 52 benzenderivater i NIR og så sammenheng mellom signalene og strukturen av forbindelsene.
- 1891 Michelson konstruerte et interferometer som dagens FTIR instrument bygger på. Hvordan interferometere virker.
- 1892 John William Strutt, Lord Rayleigh fant at Fouriertransformering av interferogrammer (tidsområdet) gav spektrum i frekvensområdet. Fouriertransformasjonen er oppkalt etter Jean Baptiste Joseph Fourier.
- 1892 Julius målte spektra av 20 organiske forbindelser fra 12800 – 1000 cm-1.
- 1898 Rubens og Aschkinass målte spektra av enkle gasser, 12800–500 cm-1, ved hjelp av KCl-prisme.
- 1900-1910. William Coblentz
- startet systematiske studier ved hjelp av IR.
- fant at forbindelser med samme empiriske formel gav ulike spektra.
- fant at like forbindelser gav like spektra.
- 1908 konstruksjon av det første IR-instrument. Prisme av NaCl. Dekket området 5000–670 cm-1.
- Perioden 1910-1930
- kvantemekanikken utvikles
- forbedring av optikk,speil, detektorer.
- IR benyttet i astronomi og fysikk.
- kjemisk interesse for IR omfattet kvalitativ analyse av funksjonelle grupper
- 1910 Wood og Trowbridge lager Echellettegitter. Echellettegitterets virkning.
- 1911 Rubens, Hollnagel og Wood publiserte det første virkelige interferogram fra IR-målinger.
- 1913 Observasjon av rotasjonsstruktur.
- 1916 Vibrerende molekyler.
- 1918 Randall og Slater laget instrument med høy oppløsning, 1 cm-1.
- 1935 Konstruksjon av IR-instrument til bruk i kjemi.
- Perioden 1939-45 betød et endelig gjennomslag for IR-spektroskopi i kjemi.
- Benyttet i til analyse av butadien/C4 fraksjon i fremstilling av syntetisk gummi. Japanernes erobring av Malaya og Nederlandsk Ost-India stanset USAs tilgang på naturgummi.
- kommersiell produksjon av IR-instrument. Beckman IR-1.
- utvikling av dobbelstråleinstrument. Instrumentets virkning.
- Roess, utviklet elektronisk vekselstrømsforsterker.
- 1941 Gildart og Wright laget en tett væskecelle med blyskille.
- 1942 McDonald introduserte nujolteknikken for faste stoffer.
- 1947 Wright og Herscher laget de første brukbare dobbelstråleinstrumentene.
- 1948 Jacquinot forstod at energimengden som når frem til prøven er større ved bruk av Michelsons interferometer enn ved bruk av monokromator.
- 1949 Fellgett utførte den første numeriske Fouriertransformering av interferogram.
- 1950 Perkin Elmer lanserte det første kommersielle dobbelstråleinstrumentet Perkin-Elmer 21.
- 1951 P.B Fellgett. Gjennom sine astronomiske observasjoner av svak stråling ved hjelp av interferometer, fant han at det såkalte signal-til-støy-forholdet (S/N) forbedret seg med en faktor tilsvarende kvadratroten av antall målinger som ble utført sammenlignet med gitterinstrumenter. Døme: På et gitterinstrument tar det 64 s for å måle et spektrum, en gang. På samme tiden kan et FT-instrument måle spektrumet 64 ganger. Forbedringen som oppnåes i S/N er kvadratroten av 64, altså 8.
- 1952 Pressing av finmalt KBr og prøve til gjennomsiktige brikker ble introdusert i Tyskland av Schiedt og Reinwein og i USA av Stimson og O'Donnell
- 1953? Mikroskop koblet til IR
- 1955 Grubb Parsons prisme/gitter dobbelstråleinstrument med stort frekvensintervall.
- 1959 Francis og Ellison målte IR spektra av monolag på metallspeil, etablerer ekstern refleksjon som ny teknikk. Til da har transmisjon vært den eneste muligheten.
- 1960/61? Fahrenfort, Harrick – utviklet intern refleksjon (ATR) IR
- 1960-65 Diffus refleksjon for kjemisk anvendelse
- 1961 Perkin Elmer laget filter/gitter dobbelstråleinstrument med stort frekvensintervall
- 1964 Research and Industrial Instruments Corp. (RIIC) produserer kommersielt FTIR med Cooley og Tukey sin hurtige Fouriertransformeringsalgoritme.
- 1967 Demonstrasjon av GC/FTIR, Intern refleksjon kommersielt tilgjengelig
- 1969 Ekstern refleksjon kommersielt tilgjengelig. Digilab lager det første fullstendig data-styrte, kommersielt tilgjengelige FTIR spektrometeret (Model FTS-14)
- 1970? NIR instrument kommersielt tilgjengelig.
Gjennom 1960 og 1970-tallet ble det utviklet hurtige Fouriertransformeringsalgoritmer (Fast Fourier Transform – FFT), integrerte kretser, datamaskiner, små gasslasere, TriGlysinSulfat detektor.
- 1980- Fouriertransformeringsinstrumenter (FTIR) blir standard, for målinger av standarder og referansespektra av reine forbindelser. Nitrogenkjølte detektorer med høy sensitivitet. Nye måleceller som bortimot eliminerer behov for prøvepreparering. Kauppinen et al. introduserer en matematisk metode for å splitte opp overlappende topper (Fourier-self deconvolution)
- 1986 Isao Noda publiserer det første arbeidet som benytter 2-dimensjonal IR spektroskopi
Litteratur[rediger | rediger kilde]
- M. Davies (Ed), Infra_red spectroscopy and molecular structure, Elsevier 1963.
- D. Lin-Vien et al., The handbook of infrared and Raman characteristic frequencies of organic molecules, Academic Press, Harcourt Brace Jovanovich Publ., 1991.
- Optical spectrochemistry, Samplings Technique Manuals, Harrick Scientific Corp., NY, 1987.
- D.A. Skoog, Principles of instrumental analysis 3. ed., CBS Colloege Publ., 1985.
- J.R. Durig (Ed), Applications of Forurier Transform Infrared Spectroscopy, Vibrational Spectroscopy and Molecular Structure, vol.18, Elsevier 1990
- P.R. Griffiths. Transform Techniques in Chemistry, Heyden, Plenum Press, NY, 1978.
- K. Janné, Near infrared reflectance spectroscopy, Lecture Notes, Biomed HB, Storvreta.
- P.R. Griffiths and J.A. de Haseth, Fourier Transform Infrared Spectroscopy, Wiley, 1986.
- J.D. Ingle and S.R. Crouch, Spectrochemical analysis, Prentice-Hall Int., 1988.
- M.W. Mackenzie (Ed), Advances in applied FTIR spec., Wiley, 1988,
- P.R. Griffiths, Chemical FT spec., Chemical Analysis, vol. 43, Wiley, 1975.
- E.G. Brame, Jr. (Ed), Applied Spectroscopy Reviews, vol. 2, Marcel Dekker, 1969.
- J. Workman, A review of process NIR: 1980-1994, J. Near infrared Spectrosc., 1, 221-45, 1993.
- F.A. Miller, Historical note of the origins of several useful IR techniques., Appl., spectrosc., 47, 7, 1096-97, 1992
- A.J. Barnes and W.J. Orville-Thomas, Vibrational spectroscopy. Modern Trends, Elsevier, 1977
- Encyclopedia of physical science and technology, Academic Press, 1992 vol. 8, pp., 110-42., vol. 13, pp. 513-4.
- Encyclopedia of spectroscopy, 1960, pp. 389-91, 446-47, 453-61.
- R.B. Barnes and R.C. Gore, Anal. Chem., 21, 1, 7-9, 1949.
- R.C. Gore, Anal. Chem., 22, 1, 7-9, 1950
- R.C. Gore, Anal. Chem., 23, 1, 7-9, 1950
- M.G. Mellon, Anal. Chem, 24, 1, 2-5, 1952
- W. Kaye, Spectrochim. Acta, 6, 257-87, 1954
- W. Kaye, Spectrochim. Acta, 7, 181-204, 1955
- M.J.D. Low and I. Coleman, Spectrochim. Acta, 22, 369-76, 1966
- Marcott, A.E. Dowrey and I. Noda, Anal. Chem., 66, 21,1065-75A, 1994
- A.L. Smith, Applied infrared spectroscopy, John Wiley, 1979
www.wooster.edu/chemistry/is/brubaker med følgende referanser:
- Beckman, A. O.; Gallaway, W. S.; Kaye, W.; Ulrich, W. F. "History of Spectrophotometry at Beckman Instruments, Inc." Anal. Chem. 1977, 49(3), 280 A-300 A.
- Griffiths, P.R. "Strong-men, Connes-men, and Block-busters or how Hertz raised the Mertz." Anal. Chem. 1992, 64(18), 868A-875A
- McDonnell, H. G., Jr. "The evolution of analytical instrumentation at Perkin-Elmer." Amer. Lab. 1980, 21, 95-101
- Miller, F. A. "The infrastructure of IR spectrometry: Reminisces of pioneers and early IR instruments." Anal. Chem. 1992, 64(17),824A-831A
- Wilks, P.A., Jr. "The evolution of commercial IR spectrometers and the people who made it happen." Anal. Chem. 1992, 64(17), 833A-838A
- Perkin-Elmer Corporation. "Instruction Manual: Perkin-Elmer infrared Equipment: Volume 3B: Model 21 infrared spectrophotometer operating and maintenance instructions" (instrument manual). The Perkin-Elmer Corporation: Norwalk, CT. 1952.
- Perkin-Elmer Corporation. "The Model 21 Double Beam Infrared Spectrophotometer: The standard instrument for infrared analysis" (sales brochure). The Perkin-Elmer Corporation* Norwalk, CT. 1953.
- Andreas Barth og Parvez I. Haris; Infrared spectroscopy – past and present. s1-52 i Biological and biomedical infrared spectroscopy. IOS Press, Amsterdam 2009. ISBN 978-1-60750-045-2
Eksterne lenker[rediger | rediger kilde]
- HyperPhysics Fysikken bak lys, optikk, fotoelektrisk effekt osb
- Physics2000 Interaktivt og pedagogisk om elektromagnetisk stråling
- Physics2000 Film om interferens
- Bioforum Animasjon av hele FTIR-prosessen
- The college of Wooster Animasjon av interferometer
- University of Colorado, Boulder Arkivert 24. oktober 2007 hos Wayback Machine. Introduksjon til tolkning av IR-spektra
- University of Colorado, Boulder Arkivert 2. juli 2007 hos Wayback Machine. IR korrelasjonstabell
- University of Colorado, Boulder Arkivert 21. november 2011 hos Wayback Machine. Øvelser i tolkning av IR-spektra
- Vidrine Consulting Infrarøde korrelasjonskart
- Spectroscopic tools Koble IR-spektra mot NMR og MS
- CALIFORNIA STATE UNIVERSITY, STANISLAUS Øvelser i tolkning av IR-spektra
- Colby College Øvelser i tolkning av IR-spektra
- Organic chemistry Online Øvelser i tolkning av IR-spektra
- Webspectra Øvelser i tolkning av IR-spektra