Emisjonsspekter
Emisjonsspekteret til et grunnstoff viser hvilke bølgelengder grunnstoffet kan sende ut. Hvert grunnstoff har sitt unike emisjonsspekter. Røntgenfluorescens (XRF) er en analysemetode til å bestemme kjemisk sammensetning til et sammensatt stoff. Emisjon betyr utsendelse, men i denne sammenheng: utstråling.
Når et stoff tilføres energi til det gløder, vil det avgi elektromagnetisk stråling som lys. Vi sier at stoffet fluorescerer. Emisjon betyr utsendelse, men i denne sammenheng: utstråling. Noe av strålingen oppfatter vi som varme og noe som lys.
Hvis vi bryter den delen av spekteret der det synlige lyset befinner seg, ved hjelp av et gjennomsiktig prisme av for eksempel glass, ser vi at det består av en rekke farger, fra rødt til fiolett, som gradvis går over i hverandre. Rødt lys har lengst bølgelengde, og minst energi mens det fiolette lyset har kort bølgelengde, og mye energi.
Ved å forstørre spekteret fra sollys, kom man for mange tiår tilbake, fram til at visse farger manglet: spekteret hadde svarte linjer. Disse linjene fikk navn etter oppdageren og kalles fortsatt for «Fraunhoferske linjer». Disse linjene viste til at noen strålefrekvenser ble absorbert eller ikke emittert.
Atomer har en positiv kjerne med protoner og nøytroner. Rundt kjernen er baner /skall/ lober for elektroner i ulike nivåer som har plass til forskjellige antall elektroner. Når ett foton med riktig bølgelengde treffer stoffet kan fotonet bli absorbert og ett elektron får mer energi ved å løftes opp i en annen elektronbane/et annet elektronskall. De mørke linjene tilsvarer frekvensen som er absorbert.
Atomspektret til et grunnstoff eller en kjemisk forbindelse er den relative intensiteten til hver frekvens i den elektromagnetiske strålingen som emiterer fra stoffets atomer eller den kjemiske forbindelsens molekyler når de faller tilbake til grunntilstanden (det vanlige energinivået). Atomspektre oppstår altså når et atom går fra et høyere energinivå til et lavere energinivå. Differansen i energi (E) mellom de to nivåene avgis i form av et foton med energi lik differansen mellom de to nivåene (E=hf, der h= Plancks konstant).
Forskjellige energioverganger gir forskjellige fotonenergier og dermed forskjellige frekvenser (f) (eventuelt bølgelengder) for fotonene. Hver frekvens gir opphav til en linje i atomspektret. Hvert stoff har sitt unike atomspekter. Spektroskopi kan derfor brukes til å identifisere ulike stoffer i en ukjent blanding. På samme måte kan spektrene av molekyler brukes i kjemisk analyse av substanser.
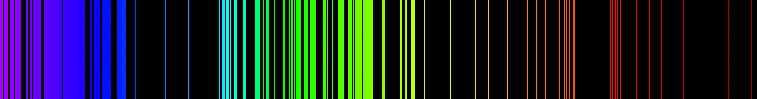
Når elektronet faller inn i et lavere, mindre energirikt skall sender det ut ett foton med bestemt bølgelengde. Dette danner striper av lys i emisjonsspekteret.

Se også[rediger | rediger kilde]
Kategori:Kvantemekanikk
