Rutherford-spredning
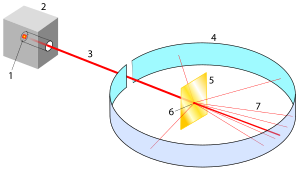
Rutherford-spredning betegner det eksperimentet som Ernest Rutherford ledet i 1911 og førte til oppdagelsen av atomkjernen. Han observerte hvordan α-partikler ble avbøyer i sin bevegelse av forskjellige atomer. Da denne spredning skyldes den frastøtende Coulomb-kraften mellom partiklene og atomkjernen, omtales også prosessen som Coulomb-spredning.
Oppdagelsen førte til at Rutherford kunne danne seg et bilde av atomet som bestående av en liten, positivt ladet atomkjerne med elektroner kretsende omkring i stor avstand fra denne. Dette var grunnlaget for Rutherfords atommodell som dermed erstattet Thomsons rosinbollemodell hvor elektronene beveget seg i en jevn bakgrunn med positiv ladning fordelt over hele atomet. Allerede i året etterpå ga Niels Bohr en matematisk beskrivelse av denne nye modellen som etterhvert utviklet seg til moderne atomfysikk.
Historie
[rediger | rediger kilde]
Da Rutherford ble ansatt ved Universitetet i Manchester i 1907, fortsatte han sine undersøkelser av egenskapene til α-partikler. Sammen med sin assistent Hans Geiger viste han at disse kunne påvises ved et ionosasjonskammer som senere ble kjent som Geiger-teller. I denne sammenheng oppdaget de at alfapartiklene ble spredt når de gikk gjennom forskjellige gasser eller materialer. Dette forundret Rutherford da han trodde at de var såpass tunge at de ville bevege seg omtrent uhindret.[1]
Allerede i 1908 publiserte Geiger de første resultatene av et eksperiment som undersøkte spredning av α-partikler mot gull eller aluminum. Disse metallene kun lett lages i tynne folier som ikke absorberte for mye stråling. Som kilde for alfapartiklene ble et lite, konisk rør inneholdende radon benyttet. Det var utført slik at kun små spredningsvinkler kunne observeres.[2]

For å undersøke muligheten for at partiklene kunne spredes til større vinkler, ble et nytt eksperiment planlagt. Her ville man se om alfastrålingen kunne reflekteres fra en metallisk flate. Den unge student Ernest Marsden ble nå knyttet til prosjektet. Den radioaktive kilden var her skjermet med en blyplate slik at kun reflekterte partikler ville kunne detekteres. De fant at en brøkdel 1/8000 partikler ble reflektert, det vil si spredt en stor vinkel.[3]
Etter dette eksperimentet gjorde Geiger i 1910 mer presise målinger av småvinkel-spredning i et forbedret vakuumrør. Ved å benytte en renere α-kilde som ga en veldefinert energi til partiklene, kunne han vise at spredning mot forskjellige metaller økte raskt med deres atomnummer. Videre kunne han redusere energien til alfapartiklene ved å la de gå litt gjennom luft og fant derav at spredning med en viss vinkel økte ved avtagende energi.[4]
Disse resultatene fikk Rutherfordi til å skrive i 1911 sitt viktige arbeid The Scattering of α and β Particles by Matter and the Structure of the Atom. Ut fra eksperimentene konkluderte han her med at α-partiklene måtte ha vært utsatt for et så sterkt elektrisk felt som tilsvarte at hele den positive ladningen i atomet var konsentrert i en liten kjerne med radius mindre enn 10-12 cm, det vil si mindre enn 1/10000 av dets størrelsen. Spredningen skyldes Coulomb-kraften mellom de innkommende partiklene og atomkjernen. Ut fra denne antagelsen beregnet han spredningstverrsnittet for prosessen og viste at det var i overensstemmelse med de oppnådde resultatene.[5]
Geiger og Marsden gikk nå i gang med å bygge opp et helt nytt eksperiment for å verifisere disse antagelsene ved nøyaktige målinger av α-spredning for vilkårlig store vinkler. Resultatene ble publisert i 1913 og ga den endelige bekreftelse av denne Rutherfords atommodell.[6]
Matematisk beskrivelse
[rediger | rediger kilde]
Når atomkjernen antas å ha elektrisk ladning Q = Ze der e er elementærladningen, gir den opphav til et elektrisk potensial Φ = Q/4π ε0r i avstand r når man benytter måleenheter i SI-systemet. En α-partikkel som befinner seg i dette punktet og har ladning q, har da en potensiell energi
Ved å innføre konstanten g = qZe/4π ε0, kan denne skrives mer kompakt som V = g/r.
Man kan anta at alfapartikkelen med masse m har hastigheten v langt borte fra atomkjernen hvor potensialet kan settes lik null. Den starter da ut med en total energi som er lik med den kinetiske energien
Da partikkelen har positiv ladning q på samme måte som kjernen, vil en partikkel som beveger seg rett mot denne, bremses opp. Ved en minste avstand d vil den helt stoppe opp og reflekteres tilbake i motsatt retning. I dette punktet er den kinetiske energien gått over til ren, potensiell energi slik at denne avstanden er d = g/E. Desto høyere hastigheten er, desto nærmere atomkjernen kommer α-partikkelen.[7]
Hyperbelbevegelse
[rediger | rediger kilde]
I sin beregning av spredningstverrsnittet for prosessen benyttet Rutherford seg av at Coulomb-kraften fra atomkjernen varierer med avstanden på samme måte som gravitasjonskraften som styrer en planet om Solen.[5] Da kraften er frastøtende, vil bevegelsen istedetfor en ellipse bli en hyperbel som for noen kometer. På samme måte som for en bunden ellipsebane, har hovedaksen en lengde a som kun avhenger av den totale energien til partikkelen og er derfor uavhengig av hvordan den nærmer seg atomkjernen. Fra det spesielle tilfelle med en sentral kollisjon har man da at d = 2a hvorav denne lengden kan uttrykkes ved hastigheten til alfapartikkelen.
For en vilkårlig kollisjon ville partikkelen ha passert atomkjernen i en avstand b fra kjernen hvis det ikke hadde vært noen spredning. Dette er kollisjonens «støtparameter». Når den er i sitt nærmeste punkt, befinner den seg i en retning gitt ved vinkelen α fra denne innkommende retningen. Den totale spredningsvinkelen er derfor θ = π - 2α. Fra geometrien til kollisjonen følger nå at
Denne sammenhengen gjør det mulig å betrakte støtparameteren b som hyperbelens imaginære akse. Den tilfredsstiller a 2 + b 2 = c 2 hvor da c er avstanden fra hyperbelens sentrum til partikkelen når den er nærmest atomkjernen. Avstanden mellom denne og partikkelen i dette spesielle punktet er derfor
For et sentralstøt er θ = π slik at rmin = 2a som forventet.
Dreieimpulsen til partikkelen er konstant under hele støtet. Hvis den har hastigheten vn i sitt nærmeste punkt, vil da vb = vn(c + a). Kvadreres denne sammenhengen, gir den
Likedan gir bevarelse av energien til partikkelen
Eliminasjon av hastigheten vn gir nå g = 2aE hvor E = mv 2/2 er partikkelens totale energi.
Spredningstverrsnitt
[rediger | rediger kilde]
Denne klassiske beregningen av bevegelsen til alfapartikkelen som Rutherford gjennomførte, kan nå benyttes til å beregne det differensielle spredningstverrsnittet for prosessen. Det gir sannsynligheten for å detektere en partikkel i et differensielt romvinkelelement dΩ = 2π sinθ dθ. Formelen
kan da benyttes der man tar absoluttverdien av den deriverte db/dθ hvis denne er negativ. Ved å benytte at nå er b = a cot(θ/2), finner man herav hvordan dette tverrsnittet varierer med spredningsvinkelen θ og den kinetiske energien E til α-partikkelen,
ved å benytte sammenhengene a = d/2 = g/2E. Det spesielle med dette resultatet til Rutherford er at man kommer frem til samme formel ved bruk av kvantemekanikk. I utgangspunktet var det ingen grunn til et slikt sammentreff.[7]
Ved de videre eksperimentene til Geiger og Marsden ble det verifisert at spredningstverrsnittene øker med kvadratet til kjerneladningen Ze og avtar som 1/v4 med hastigheten til partiklene. På samme ble vinkelvariasjonen 1/sin4(θ/2) funnet å være i overensstemmelse med de eksperimentelle resultatene.[6]
Referanser
[rediger | rediger kilde]- ^ A. Pais, Inward Bound, Oxford University Press, England (1986). ISBN 0-19-851971-0.
- ^ H. Geiger, On the scattering of the α-particles by matter, Proc. Roy. Soc. A 81 (546), 174–177 (1908).
- ^ H. Geiger and E. Marsden, On a Diffuse Reflection of the α-Particles, Proc. Roy. Soc. A 82 (557), 495–500 (1909).
- ^ H. Geiger, The scattering of α-particles by matter, Proc. Roy. Soc. A 83 (565), 492–504 (1910).
- ^ a b E. Rutherford, The Scattering of α and β Particles by Matter and the Structure of the Atom, Phil. Mag. Series 6, 21, 669-688 (1911).
- ^ a b H. Geiger and E. Marsden, The Laws of Deflexion of α Particles through Large Angles, Phil. Mag. Series 6, 25, 604–623 (1913).
- ^ a b R.M. Eisberg, Fundamentals of Modern Physics, John Wiley &. Sons, New York (1965).
Eksterne lenker
[rediger | rediger kilde]- (en) Rutherford scattering – kategori av bilder, video eller lyd på Commons
- AIP, Alpha Particles and the Atom, historisk bakgrunn.
- HyperPhysics, Rutherford scattering, innholdsrike nettsider.
- M. Fowler, Rutherford scattering, forelesninger ved University of Virginia.








